리튬: 원소 속성 및 용도
원소 리튬에 대한 이해
리튬이란 무엇인가요?
원자 번호 3번, 기호 Li인 리튬은 주기율표에서 가장 가벼운 금속이자 알칼리 금속입니다. 2세기 동안 실험실의 호기심으로 존재했던 리튬은 전 세계적으로 거래되는 산업 상품으로 발전했습니다. 오늘날, 소금의 전기분해나 스포두멘과 같은 광물의 제련을 통한 리튬 정제 및 생산은 에너지 저장, 우주 탐사 및 전자 산업에서 수십억 달러 규모의 산업의 기반이 되고 있습니다.

화학적 특성 설명
리튬의 화학적 특성은 물리적 특성과 마찬가지로 독특한 특징을 지니고 있습니다:
-반응성: 리튬은 물과 격렬하게 반응하여 수산화리튬(LiOH)과 수소 가스를 형성합니다. 예를 들어, 작은 리튬 조각을 물에 담그면 몇 초 안에 눈에 보이는 기포가 생길 수 있습니다.
-알칼리성: 또 다른 알칼리 금속인 리튬은 외부 전자 하나를 쉽게 내어주어 Li⁺ 이온을 생성하므로 리튬 이온 배터리를 비롯한 전기화학 반응에서 중요한 역할을 합니다.
- 가연성: 리튬은 특유의 붉은 불꽃으로 발화하므로 엔지니어는 벌크 리튬을 작업하고 보관할 때 이 점을 염두에 두어야 합니다.
물리적 특성 데이터 표
|
속성 |
값 |
|
원자 번호 |
3 |
|
원자 무게 |
6.94 g/mol |
|
녹는점 |
180.54 °C |
|
끓는점 |
1590 °C |
|
밀도 |
0.534 g/cm³ |
|
외관 |
은백색 금속 |
|
경도 |
Soft |
|
전기 전도도 |
높음 |
|
열 전도성 |
높음 |
리튬의 발견
리튬은 1817년 스웨덴 우토의 섬 페탈라이트에서 처음 발견되었습니다. 아르프베드손의 분석 결과 나트륨이나 칼륨 이외의 성질을 가진 미지의 새로운 원소가 밝혀졌습니다. 이후 리튬 염의 전기분해를 통해 금속 리튬이 분리되었고, 과학자와 엔지니어들은 리튬의 물리적, 화학적 특성을 더 자세히 분석할 수 있었습니다. 시간이 지나면서 리튬의 가벼움, 높은 반응성, 전기화학적 잠재력이 결합되어 에너지 저장에서 산업용 그리스와 의약품에 이르기까지 리튬은 다양한 분야에서 활용되기 시작했습니다.
합금과 리튬 화합물
- 리튬-알루미늄 합금: 매우 가볍고 단단하여 항공기 부품과 스포츠카 부품에 사용됩니다.
- 리튬-구리 합금: 향상된 전기 전도성을 부여하며 전자 커넥터 및 회로에 자주 사용됩니다.
- 리튬-철 인산염(LiFePO₄): 안정성과 긴 사이클 수명으로 인해 전기 자동차 배터리 음극에 일반적으로 사용됩니다.
- 수산화리튬(LiOH) 및 탄산염(Li₂CO₃): 충전 배터리, 윤활 그리스 및 산업용 화학 공정에서 매우 중요합니다.
- 염화리튬(LiCl): 건조제, 에어컨, 화학 합성에 사용됩니다.
예를 들어, Tesla 및 기타 전기 자동차 제조업체는 안전과 기능을 보장하기 위해 열 안정성과 에너지 밀도가 가장 중요한 특정 차량에 리튬인산철(LFP) 배터리를 사용합니다.
일반적인 애플리케이션
리튬의 용도는 다양합니다:
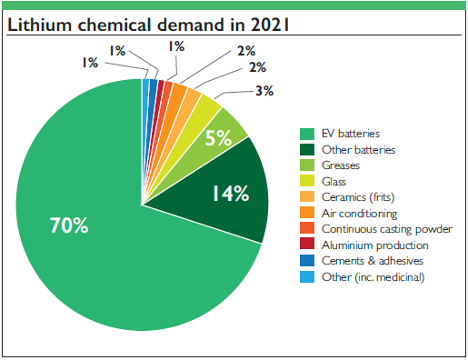
1. 배터리: 리튬 이온 및 리튬 폴리머 배터리는 높은 에너지 밀도로 인해 휴대용 전자기기, 전기 자동차 및 재생 에너지 저장 시스템에서 시장을 지배하고 있습니다.
2. 합금: 리튬은 알루미늄과 구리 합금을 경량화하여 강도를 잃지 않으면서도 항공 우주 효율성을 향상시킵니다.
3. 의약 용도: 탄산리튬은 양극성 장애 환자를 안정시키는 등 리튬이 산업적 용도를 넘어선 영향력을 보여줍니다.
4. 내열 유리 및 세라믹: 리튬은 열충격 저항성과 강도를 향상시킵니다.
5. 윤활 그리스: 리튬 그리스는 제조 및 자동차 산업에서 필수적인 고온 및 고압에서 우수한 성능을 발휘합니다.
 [1]
[1]
준비 과정
리튬은 주로 다음을 통해 얻습니다:
1. 리튬 금속은 전기분해를 통해 LiCl 또는 LiF에서 회수하여 시장 응용 분야에 적합한 고순도로 생산합니다.
2. 광물 채굴: 스포두민과 페탈라이트를 가공하여 탄산리튬 또는 수산화리튬을 만들어 배터리 및 화학 제품 생산에 사용합니다.
자주 묻는 질문
리튬의 가장 빈번한 용도는 무엇인가요?
주로 충전식 배터리, 경합금, 윤활 그리스 및 의약품에 사용됩니다.
리튬은 어떻게 채굴되나요?
리튬 염의 전기분해를 통해 또는 스포두멘 광석에서 채굴합니다.
리튬은 반응성이 있나요?
네, 특히 물과 반응하여 LiOH와 수소 가스를 형성합니다.
리튬 이온 배터리란 무엇인가요?
높은 에너지 밀도와 긴 수명 덕분에 스마트폰, 노트북, 전기 자동차, 재생 에너지 저장 시스템에 전력을 공급합니다.
참조:
[1] 국제 리튬 협회(2023년 10월 13일). 리튬 101. 검색된 날짜: 2025년 7월 17일, https://lithium.org/lithium-101/

 바
바
 비즈 & 구체
비즈 & 구체
 볼트 및 너트
볼트 및 너트
 도가니
도가니
 디스크
디스크
 섬유 및 원단
섬유 및 원단
 영화
영화
 플레이크
플레이크
 폼
폼
 호일
호일
 과립
과립
 벌집
벌집
 잉크
잉크
 라미네이트
라미네이트
 덩어리
덩어리
 메시
메시
 메탈라이즈드 필름
메탈라이즈드 필름
 플레이트
플레이트
 파우더
파우더
 Rod
Rod
 시트
시트
 단결정
단결정
 스퍼터링 타겟
스퍼터링 타겟
 튜브
튜브
 워셔
워셔
 전선
전선
 변환기 및 계산기
변환기 및 계산기
 글쓰기
글쓰기




 Chin Trento
Chin Trento



