MoO3 나노 입자에 대해 알아야 할 모든 것
소개
삼산화몰리브덴은 화학식 MoO3(H2O)n(n=0~3)을 갖는 전이 금속 산화물 중 하나입니다. MoO3는 광촉매, 광학, 가스 감지, 배터리, 전자 기기 등 다양한 응용 분야에 사용됩니다. 무수 MoO3는 왜곡된 "MoO6" 팔면체 구조를 만듭니다. 그림 1은 사면체 결정을 나타냅니다. 녹색 구체는 몰리브덴이고 빨간색 구체는 산소입니다. MoO3는 α-정사면체, β-단사면체, h-육면체의 세 가지 결정 구조를 가지고 있습니다. MoO3의 구조가 다르면 물리적, 화학적 특성이 달라집니다. h-MoO3는 436℃까지 상 안정성을 보이지만 α-MoO3는 436℃ 이하에서 비가역적인 상 전이를 보입니다[1].

그림 1: MoO6 팔면체 구조
MoO3 나노 구조의 제조 방법 및 용액 연소 합성 논의
삼산화몰리브덴 나노 입자를 제조하는 합성 방법에는 여러 가지가 있습니다:
수열 합성: 몰리브덴산 암모늄과 같은 몰리브덴 염이 고온, 고압의 수용액에서 과산화수소와 반응하여 MoO3 나노 입자를 형성합니다.
용매 합성: 몰리브덴 염이 고온 환경에서 에탄올과 같은 유기 용매와 반응하여 MoO3 나노 입자를 형성합니다.
공침: 몰리브덴 염 용액이 특정 pH에서 금속 수산화물 또는 탄산염과 같은 침전제와 반응하면 용액에서 MoO3 나노 입자가 침전됩니다.
용액 연소 합성: 몰리브덴 염을 연료 산화제 혼합물과 혼합하고 고온에서 연소시켜 MoO3 나노 입자를 형성합니다.
여기에 언급되지 않은 다른 많은 합성 방법이 있습니다. 더 자세한 정보나 관심이 있으시면 Stanford Advanced Materials에 문의해 주세요. 한 번의 합성에서도 다양한 파라미터에 따라 다양한 종류의 나노 MoO3 구조가 만들어집니다. 용액 연소 합성을 예로 들어 보겠습니다.
암모늄헵타몰리브덴산염(NH4)6Mo7O24-4H2O를 증류수에 녹이고 용액을 유기 용매와 혼합합니다(여기서는 실험을 위해 다양한 유기 첨가제로 우레아, EDTA, PEG 200 및 소르비톨을 사용합니다). 침전물이 형성될 때까지 용액을 가열하고 저어줍니다. 마지막 단계는 침전물을 가열하여 유기 첨가제 및 기타 불순물을 제거하는 것입니다[2].
암모늄 헵타몰리브덴산염(AHM)은 Mo 화합물 생산의 전구체로 자주 사용되는 대형 복합 분자입니다. AHM의 용액 연소 합성 화학 방정식은 다음과 같습니다.
MoO3는 첨가제를 사용하지 않고도 형성될 수 있지만, 첨가제는 결정 성장과 MoO3 핵을 유도하는 데 중요한 역할을 합니다. 주사 전자 현미경(SEM)을 사용하여 다양한 유기 첨가제를 사용하여 생성된 미세 구조를 감지합니다. 다음과 같은 관찰 결과를 얻었습니다: 우레아는 다른 3가지 첨가제보다 더 구형의 형태를 만듭니다. PEG 200은 더 큰 서브 마이크로와 덜 구형의 나노 입자를 만듭니다. 소르비톨과 EDTA는 상당히 다른 나노막대를 만듭니다[2]. 이는 유기 첨가제의 화학 구조로 인해 발생합니다. 아래 그림 2는 이 네 가지 유기 첨가제의 화학 구조를 보여줍니다. 우레아는 비결합 전자 쌍을 가진 질소를 가지고 있습니다. PEG200과 소르비톨은 OH 그룹에 산소가 있습니다. EDTA는 비결합 전자 쌍을 가진 질소와 OH 그룹에 산소를 모두 가지고 있습니다. 리간드 형성에서 자유 전자가 2개인 질소는 산소보다 많습니다. 따라서 요소는 PEG200 및 소르비톨에 비해 더 작은 크기의 핵을 형성하기 위해 AHM에서 Mo를 끌어 당기는 것이 더 쉽습니다 [2].
EDTA는 2 개의 자유 전자를 가진 2 개의 질소와 OH에 4 개의 산소를 가지고 있습니다. 첫 번째 관점에서 MoO3 나노 입자를 만드는 데 가장 적합한 첨가제일 수 있습니다. 그러나 EDTA는 앞서 언급했듯이 매우 큰 복합 화합물입니다. 입체 방해 효과는 EDTA의 질소가 Mo를 끌어당기는 것을 방해합니다. 산소기만 리간드 구조에 관여하여 MoO3의 미세 구조를 만듭니다[2].
PEG200은 양쪽에 산소기만 있습니다. 요소만큼 매력적이지 않기 때문에 양쪽에서 동시에 MoO3를 형성할 가능성이 낮습니다. 그러나 PEG200은 입체 방해 효과가 낮은 매우 단순한 구조의 화합물입니다. PEG 200은 EDTA보다 리간드 형성이 더 쉽습니다[2].
소르비톨의 산소기 중 하나가 Mo와 결합하면 선형 구조로 인해 다른 산소기가 다른 Mo와 결합하는 것이 불가능합니다. 따라서 모든 소르비톨은 MoO3 나노 입자를 만드는 데 좋은 첨가제가 아닙니다[2]. pH, 반응 온도, Mo 농도, Mo/첨가제 비율과 같은 다른 조건도 생산된 MoO3 나노입자의 특성에 영향을 미칠 수 있습니다.
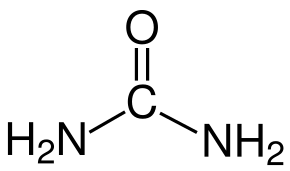
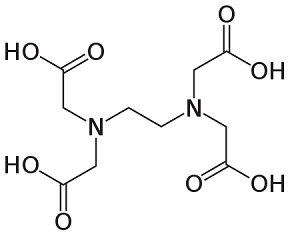
요소 EDTA
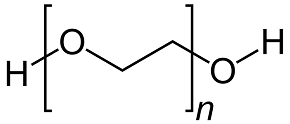
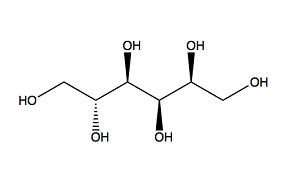
PEG200 소르비톨
그림 2: 실험에 사용된 유기 첨가제의 분자 구조
MoO3 응용 분야
MoO3 멤브레인은 전기 변색 특성이 우수합니다. WO3 및 TiO2와 같은 다른 재료에 비해 MoO3는 반응 시간이 짧습니다. 또한 MoO3는 전기 자극을 감지하면 회색으로 변합니다. 흡수 곡선은 가시 영역 내에서 매끄럽습니다. 흡수 피크는 사람의 눈의 민감한 대역에 가까운 550nm에 가깝습니다. MoO3 나노 입자로 최고의 MoO3를 만드는 방법은 가장 인기 있는 연구 중 하나입니다.
PVC는 널리 사용되는 열가소성 고분자 소재이지만 연소 시 짙은 연기를 발생시킵니다. 전이 금속은 우수한 연기 억제 효과를 보여줍니다. 두 종류 이상의 전이 금속 화합물을 결합하면 PVC의 짙은 연기를 심각하게 제한할 수 있습니다. PVC는 가소제를 첨가하기 때문에 사용 시 심각한 화재 위험이 있습니다. MoO3는 또한 우수한 난연성을 보여줍니다. MoO3와 Cu2O를 결합하면 순수 MoO3 첨가제 비용을 절감하고 케이블의 우수한 특성을 유지할 수 있는 시너지 효과를 발휘합니다.
MoO3는 고효율 광촉매입니다. 기존의 폐수 염료 처리와 달리 나노 광촉매는 오염 물질을 CO2와 같은 무해한 제품으로 전환할 수 있습니다[3]. 나노 입자는 MoO3에 더 많은 접촉 면적을 제공하여 더 빠른 분해 속도를 제공합니다.
MoO3는 가스 감지와 같은 광범위한 애플리케이션에 사용할 수 있는 n형 반도체입니다. 금속 산화물 가스 감지기는 다른 감지기보다 더 빠르고 간단하게 가스를 전기로 "전달"합니다. 다른 금속 산화물 가스 감지기와 달리 MoO3는 표면에 측정할 가스와 선택적으로 반응하는 활성 부위가 있는 와이드 밴드갭 반도체 소재입니다. MoO3는 가스에 민감한 특성을 가지고 있습니다. 약 450℃에서 NH3, H2, CO 및 기타 가스에 대한 민감도를 보여줍니다. 순수한 MoO3 멤브레인은 온도와 선택성이 매우 민감하기 때문에 잘 작동하지 않습니다. 다른 물질과 결합하여 MoO3 가스 감응 능력을 향상시킬 수 있습니다. 예를 들어 MoO3와 V2O5를 결합하여 멤브레인을 만들면 저온(약 150℃)에서 NO2, NH3, CO, CH4, SO2, H2에 대해 높은 감도를 보입니다.
언급되지 않은 MoO3 나노 입자의 응용 분야는 많습니다. Stanford Advanced Materials (SAM)는 다양한 종류의 MoO3를 제공합니다. MoO3에 대한 자세한 정보를 원하시면 기술 담당자에게 애플리케이션 정보를 제공하여 조언을 구할 수 있습니다.
참고 자료
- 판니파 웡크루아, 티티푼 통템, 솜차이 통템, "환류 및 결합 조합에 의한 h- 및 α-MoO3의 합성: 상 및 형태 변환, 광촉매 및 광감작", Journal of Nanomaterials, 2013, 논문 번호 702679, 8 페이지, 2013. https://doi.org/10.1155/2013/702679
- 파비즈, D., 카즈→에메이니, M., 라시디, A. M., & 자파리 조자니, K. (2009). 형태 및 크기 제어를 이용한 용액 연소 방법에 의한 MOO3 나노 구조의 합성 및 특성화. 나노 입자 연구 저널, 12(4), 1509-1521. https://doi.org/10.1007/s11051-009-9727-6
- Thekkethil, A. J., Sreekuttan, S., & Madhavan, A. A. (2021). 열 저장 및 광촉매에 나노 삼산화 몰리브덴의 적용. 물리학 저널: 컨퍼런스 시리즈, 2070(1), 012120. https://doi.org/10.1088/1742-6596/2070/1/012120

 바
바
 비즈 & 구체
비즈 & 구체
 볼트 및 너트
볼트 및 너트
 도가니
도가니
 디스크
디스크
 섬유 및 원단
섬유 및 원단
 영화
영화
 플레이크
플레이크
 폼
폼
 호일
호일
 과립
과립
 벌집
벌집
 잉크
잉크
 라미네이트
라미네이트
 덩어리
덩어리
 메시
메시
 메탈라이즈드 필름
메탈라이즈드 필름
 플레이트
플레이트
 파우더
파우더
 Rod
Rod
 시트
시트
 단결정
단결정
 스퍼터링 타겟
스퍼터링 타겟
 튜브
튜브
 워셔
워셔
 전선
전선
 변환기 및 계산기
변환기 및 계산기



 Chin Trento
Chin Trento



